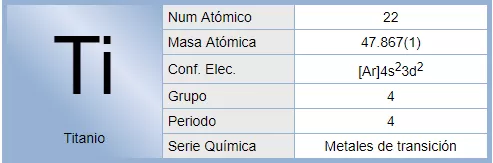
El titanio es un elemento químico de símbolo Ti y número atómico 22 que se sitúa en el grupo 4 de la tabla periódica de los elementos. Es un metal de transición de color gris, baja densidad y gran dureza. Es muy resistente a la corrosión por agua del mar, agua regia y cloro.
En estado puro, presenta una elevada resistencia a la corrosión y la mayor proporción de dureza-densidad de todos los elementos metálicos. El titanio es tan fuerte como algunos aceros, pero su densidad es menor. Tiene dos formas alotrópicas y cinco isótopos naturales que van desde 46Ti hasta 50Ti, siendo 48Ti el más abundante de ellos.
Abundancia
El titanio siempre ocurre naturalmente unido a otros elementos. Es el noveno elemento y séptimo metal más abundante en la corteza terrestre, suponiendo un 0,63 % de su masa. Está presente en la mayoría de rocas ígneas y sedimentarias, así como en diversas formas de vida y cuerpos de agua naturales.
Su aparición se produce principalmente en los minerales anatasa, brookita, ilmenita, perovskita, rutilo y titanita. todos estos minerales, solo el rutilo y la ilmenita presentan importancia económica, a pesar de ser difícil de encontrar en altas concentraciones.
Isótopos
Se encuentran 5 isótopos estables en la naturaleza: 46Ti, 47Ti, 48Ti, 49Ti e 50Ti, siendo 48Ti el más abundante de ellos con un 73,8% de abundancia natural. Se caracterizaron once radioisótopos, siendo los más estables 44Ti con un período de semidesintegración de 63 años, 45Ti con un período de 184,8 minutos, 51Ti con un período de 5,76 minutos y 52Ti con un período de 1,7 minutos. Para el resto, sus vidas medias son de menos de 33 segundos, y la mayoría de menos de medio segundo.
Aplicaciones
- El titanio se emplea en las aleaciones de acero para reducir la cristalidad y como desoxidante, y en las de acero inoxidable para reducir su contenido de carbono. Son frecuentes también las aleaciones con aluminio, vanadio, cobre, hierro, manganeso, molibdeno y otros metales.
- El metal de titanio se utiliza en diversas aplicaciones en la automoción, particularmente en el automovilismo y el motociclismo, donde la reducción de peso manteniendo la resistencia y rigidez es un factor crítico.
- Es habitual el uso del titanio en los diseños de joyería, gracias a su durabilidad y propiedades inertes que hacen de este metal una buena elección para evitar posibles alergias y resistir al agua.
- El titanio se emplea también en muchos aparatos deportivos, como por ejemplo raquetas de tenis, palos de golf, mangos de los palos de lacrosse, rejas para cascos de cricket, hóckey, lacrosse y fútbol americano, y marcos y componentes de bicicletas.
Precauciones
El titanio no es tóxico aún en grandes dosis y no juega ningún rol biológico natural en el cuerpo humano. Se estima que los humanos ingieren una cantidad de 0,8 miligramos de titanio cada día, aunque en su mayoría es expulsado posteriormente sin que el cuerpo lo absorba. Sin embargo, el titanio sí tiene tendencia a acumularse biológicamente en tejidos que contienen sílice, y un estudio de 2011 indicó una posible conexión entre el titanio y el síndrome de la uña amarilla